
载体构建(vectorconstruction)是把连接好的DNA分子运送到受体细胞中去。首先,必须寻找一种能进入细胞、在装载了外来的DNA段后仍能照样复制的运载体。理想的运载体是质粒(plasmid),在基因工程中,常用人工构建的质粒作为载体。当给质粒插入一段外源DNA段后,它依然能够进行自我复制。载体构建是分子生物学研究常用的手段之一。
1.载体构建
载体构建(vectorconstruction):载体构建是分子生物学研究常用的手段之一。主要包括已有载体多克隆位点(MCS)的改造和已有载体启动子、增强子、筛选标记等功能元件的改造。是为把DNA分子运送到受体细胞中去,必须寻找一种能进入细胞、在装载了外来的DNA片段后仍能照样复制的运载体。理想的运载体是质粒(plasmid),在基因工程中,常用人工构建的质粒作为载体。载体构建即是构建含外源DNA的质粒。
特点:当给质粒插入一段外源DNA片段后,它依然能够进行自我复制。
2.多克隆位点
多克隆位点(multiple cloning site, MCS),指的是包含数个(最多20个)限制性酶切位点(restriction site)的一段很短的DNA序列。也称为多位点接头(polylinker),是基因工程中常用到的载体质粒的标准配置序列。MCS上含有多个单一酶切位点,是外源DNA的插入部位,每个限制性酶切位点通常是唯一的,即它们在一个特定的载体质粒中只出现一次。不同酶的酶切位点可有重叠。单一酶切位点就是只有一种特定的酶能够识别并进行酶切的位点,多克隆位点一般是位于质粒上的一段序列,这段序列含有很多个酶切位点,但这些酶切位点每一个都被一种酶识别并酶切。
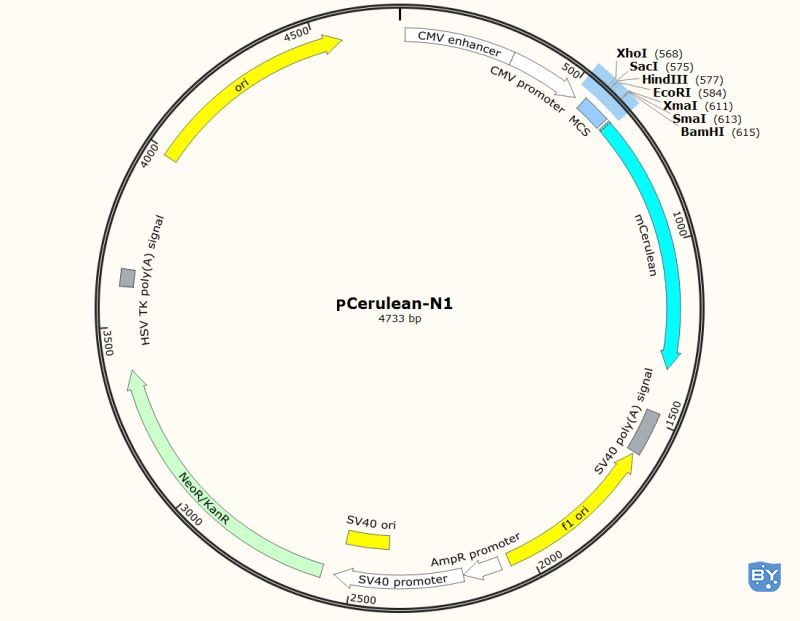
3.质粒构建
(1)质粒构建原理
质粒构建是分子生物学研究中最常用的实验技术。原理依赖于限制性核酸内切酶,DNA连接酶和其他修饰酶的作用,分别对目的基因和载体DNA进行适当切割和修饰后,将二者连接在一起,再导入宿主细胞,实现目的基因在宿主细胞内的正确表达。
(2)质粒构建方式
质粒构建方式多样,常规的T4连接酶,下面就介绍下T4连接酶构建质粒方法,T4连接酶可用于平末端也可用于粘性末端连接,但一般推荐适用黏性末端。
(3)质粒载体的制备
质粒载体的制备既可以选择单酶切也可以选择双酶切,一般推荐使用双酶切。其实目的就只有一个,尽量使载体的末端具有特异性,防止自连。
4.一般目的基因用于克隆表达的情况下,酶切位点的选择要考虑到:
(1)选择质粒上两个酶切位点的距离不应小于太小(>10bp),否则影响限制性内切酶对切点的识别,不利于空载体的双酶切。
(2)一般目的基因用于克隆表达的情况下,酶切位点的选择要考虑到:
目的基因片段内部不含有所选的酶切位点(不然鉴定阳性重组子双酶切时会将目的基因切断)。
(3)实验后继应用的所有载体(真核、原核、酵母、昆虫)都尽可能含有所选的酶切位点。并且要保证在载体上的插入方向正确(定向克隆)。(不然换载体表达时,还要重新设计引物,以引进新的酶切位点)。
(4)尽可能选比较常用的酶切位点(常用切点酶的价格比较便宜)。
(5)两个酶切点至少隔上3个碱基。
(6)两个酶切点最好不要是同尾酶(切下来的残基不要互补),否则效果相当于单酶切。
(7)最好使用酶切效率高的酶。
(8)最好使用双酶切有共同buffer的酶。
 文章推荐
文章推荐